对癌症病人实现快速、简便地早期筛查是医疗界的迫切需要。近日,威廉希尔中文网站平台顾金楼教授团队,报道了基于可调介孔的分级结构金属有机骨架,构建特异性酶促反应的传感模型,实现前列腺癌病人(PCa)的精准筛选。该工作只需要采集病人一滴尿液,即可快速、准确的筛查癌症病人,可避免传统PSA和肛检方法复杂尴尬的过程。系列工作已申请专利(202110648627.8),随后课题组将部分数据发表在《美国化学会志》(J. Am. Chem. Soc. DOI: 10.1021/jacs.1c05674)上。
PCa是严重影响男性健康的最常见癌症之一。对于大多数患者来说,在早期阶段没有明显的临床症状,因此PCa的早期筛查对于改善患者的生活质量和降低其死亡率至关重要。肌氨酸被证实为早期PCa的临床标志物,通过对尿液中的肌氨酸水平进行检测可完成简单和无创的早期PCa诊断。然而,在PCa的病理过程中,人类尿液中的肌氨酸含量仅增加不到一个数量级。此外,探针通常容易受到临床样本中可能共存的大量生物分子的干扰。因此,很难准确区分肌氨酸的微小浓度变化,从而导致假阳性/阴性诊断的风险。这些问题使得临床样本中肌氨酸的特异检测具有挑战性。
针对上述问题,课题组通过间接量化临床尿样中的肌氨酸来筛查PCa个体。如图所示,该策略以肌氨酸氧化酶(SOX)作为特异性识别单元,氧敏感分子作为信号报告分子,新开发的分级介孔锆基金属有机骨架(HMUiO)具有连续可调的介孔尺寸,确保了SOX 和响应单元分别在其相邻的介孔和微孔域中空间分离的协同工作。高达 12.1 nm 的大介孔不仅大大提高了SOX的负载能力,而且为肌氨酸的自由扩散留出了足够的空间。基于此,该探针可准确检测PCa患者与健康人尿样中肌氨酸浓度的微小变化。
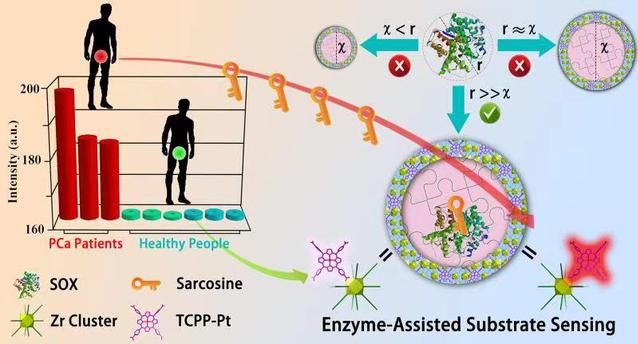
传感器量化肌氨酸用于早期前列腺癌筛选的示意图
这种基于特异性酶促反应的传感模型可有效避免结构相似的生物分子的干扰。此外,通过改变封装酶的类型,可以便捷的扩展这种酶辅助底物传感的概念,有望为合理设计多种探针以量化复杂生物样品中的特定生物标志物提供指导。
论文的第一作者为威廉希尔williamhill博士研究生赵丽玮同学,通讯作者为顾金楼教授,该研究得到了国家自然科学基金和上海市自然科学基金的支持。
论文链接:https://pubs.acs.org/doi/10.1021/jacs.1c05674
